Factos sobre os isótopos
Os átomos são os blocos de construção da vida. Constituem tudo e qualquer coisa no mundo, ou mesmo no universo conhecido. Os átomos são constituídos por protões, neutrões e electrões.
Cada elemento da tabela periódica tem o seu próprio número específico, que corresponde ao número de protões que os átomos que compõem esse elemento terão.
O mesmo se aplica ao número de electrões que se encontram nestes átomos, uma vez que este número coincide sempre com o número de protões.
O que são isótopos?
A única coisa que pode ser diferente em dois átomos do mesmo elemento é o número de neutrões que cada um contém.
Se um conjunto de átomos do mesmo elemento tiver um número diferente de neutrões, são designados por isótopos desse elemento.
No entanto, é preciso ter em conta que, mesmo que um conjunto de átomos tenha um número diferente de neutrões, continuam a pertencer ao mesmo elemento.
Mas serão designados por isótopos desse elemento, em vez de simples átomos.
Como são designados os isótopos?
Como acabou de ler, a alteração do número de neutrões não altera nem afecta a química do elemento, porque os neutrões são neutros, ou seja, não têm carga.
O único efeito que o número de neutrões tem num átomo é que podem causar uma alteração na massa.
Os isótopos são, portanto, identificados pela sua massa, que é o número total de protões e neutrões no núcleo do átomo.
Os isótopos são normalmente escritos de uma de duas formas.
Independentemente da forma como se escreve um isótopo, escreve-se a sua massa, que é novamente o número de protões e neutrões combinados.

Podem ser escritos com a massa em primeiro lugar:
14C
235U
Ou a massa pode ser escrita após o nome do elemento e um hífen, assim:
Carbono-14
Urânio-235
Todos os elementos contêm isótopos?
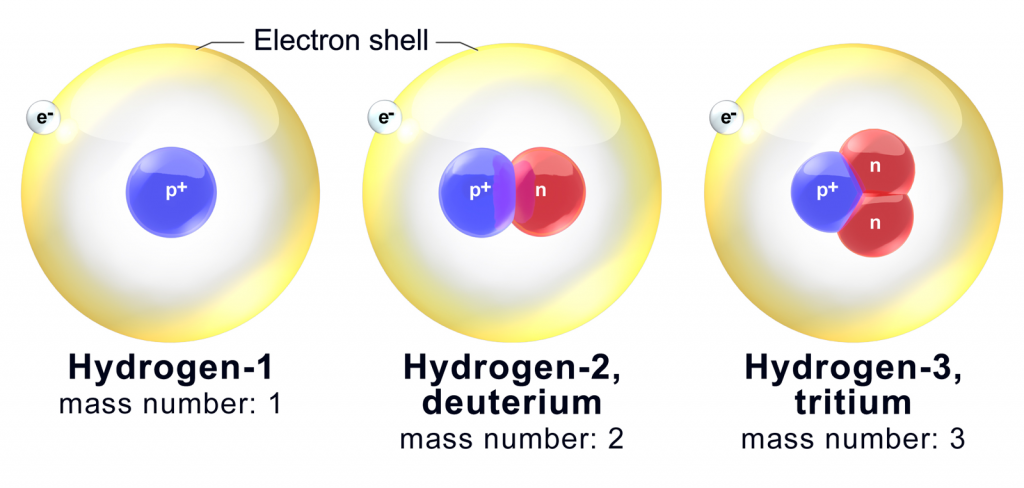
Todos os elementos têm alguns isótopos, mas o hidrogénio tem apenas três, o que é de longe o número mais reduzido.
O césio e o xénon são os isótopos que ocorrem mais naturalmente, pois cada um tem 36 que foram observados.

Isótopos estáveis e instáveis
Quando se trata de classificar um isótopo como estável ou instável, basta ver durante quanto tempo ele se mantém.
Se o isótopo só existe durante um curto período de tempo antes de decair, então é instável. Uma vez decaído completamente, estes isótopos serão um isótopo diferente ou um elemento completamente diferente.
Estes isótopos instáveis são considerados radioactivos.
A maior parte dos elementos encontrados na natureza são constituídos por isótopos estáveis.

Este tipo de isótopo é resistente à mudança e, geralmente, mantém-se durante um bom período de tempo sem se degradar.
O estanho tem o isótopo mais estável de todas as substâncias que ocorrem naturalmente, com cerca de dez isótopos estáveis na sua estrutura.
Química